研究背景
纳米颗粒作为新一代药物载体近年来在新冠疫苗、肿瘤治疗等领域正在发挥着不可替代的作用。纳米颗粒的大小、形状和表面状态等特性已被证明能够显著影响其被肿瘤细胞吞噬的效率,从而决定了纳米药物在肿瘤治疗中的作用。然而,纳米颗粒的硬度鲜有人研究,特别是在涉及到纳米颗粒主动或被动靶向癌细胞的情况下,其对细胞内吞的影响尚不清楚。另外,要获得粒径、形状和表面电荷等特性都相同而只有硬度不同的纳米颗粒,是特别困难的一件事情。
工作简介
液态金属是一种不定型、可流动的液体的金属。amjs澳金沙门线路叶坚教授团队利用液态金属纳米颗粒,基于前期所积累的颗粒氧化控制技术(Advanced Materials Interfaces, 2021, 8, 2001874)和表层二氧化硅修饰,获得了具有相同粒径、形状和表面电荷特性但不同硬度的液态金属纳米颗粒(LMNPs)。这些液态金属纳米颗粒是用于研究上述的硬度依赖性细胞内吞效应最理想的颗粒类型之一。

研究发现,在靶向性的透明质酸-CD44这一配体-受体相互作用下,较软的纳米颗粒的内吞速率比较硬的颗粒慢得多。有趣的是,一旦这种相互作用被抑制,即颗粒与细胞被动结合并内吞,较硬的颗粒反而会比较软的颗粒更快被细胞摄取。
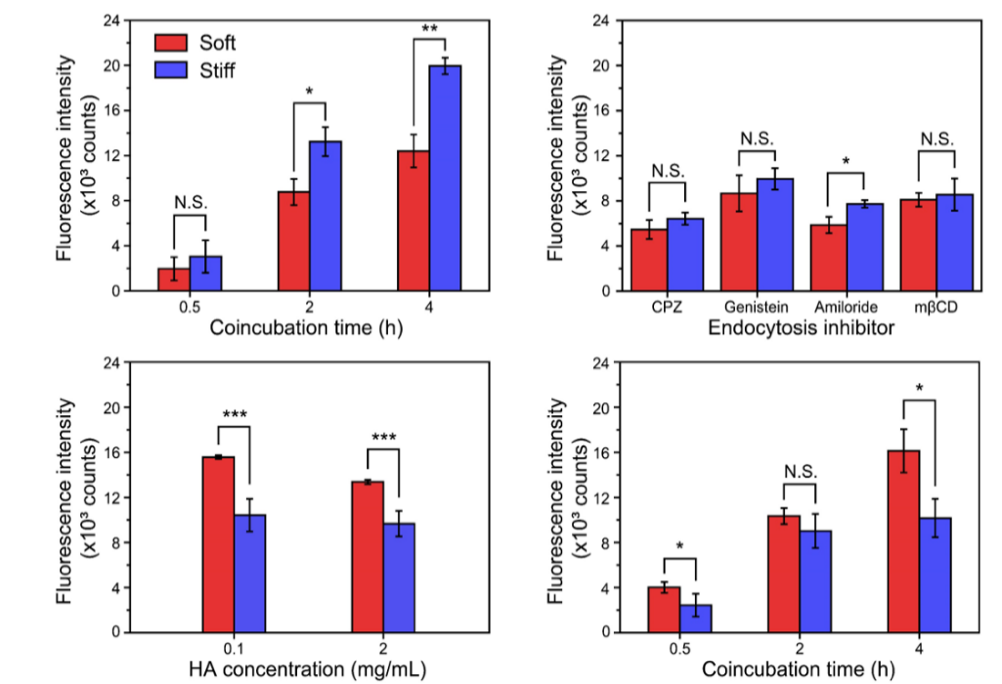
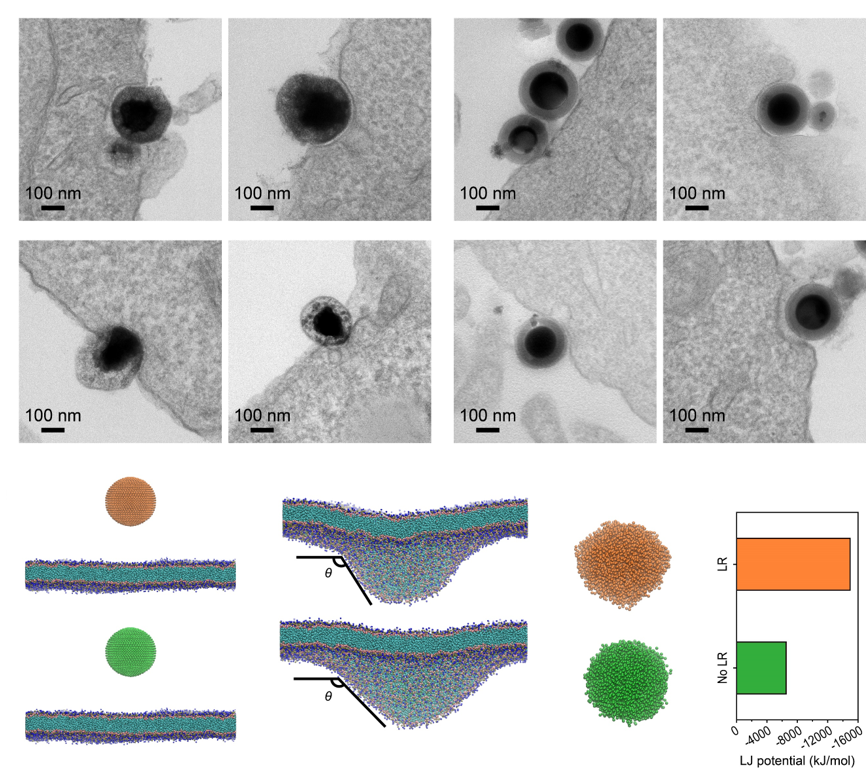
该团队进一步通过实验和模拟对纳米颗粒内吞过程中的形态变化进行了研究,结果表明柔软的颗粒更容易变形以适应细胞膜上的内吞凹陷位点,因此在颗粒与细胞膜之间没有配体-受体相互作用的情况下可以被更有效地内吞。但当配体与受体之间存在较强的亲和力时,可变形的软性颗粒能够响应内吞位点周围受体结合力,从而倾向被拉伸平铺于膜表面,导致其内吞速率比不变形的刚性NPs慢。分子动力学模拟结果也证实了软质颗粒的水平延伸性较强。这些有趣的发现清楚地表明,在主动或被动靶向策略中,肿瘤细胞对不同硬度的纳米颗粒的摄取能力是不同的。这些发现将为开发高效合理的纳米药物载体提供极具意义的指导。该工作近期发表在Nanoscale期刊上,题为The Stiffness-Dependent Tumor Cell Internalization of Liquid Metal Nanoparticles。
作者团队简介:
论文第一作者为amjs澳金沙门线路已毕业博士贺靖,论文通讯作者为amjs澳金沙门线路叶坚教授。北京航空航天大学医工交叉创新研究院林绪波教授与amjs澳金沙门线路顾波波教授参与指导。
叶坚教授课题组主页:http://www.yelab.sjtu.edu.cn
供稿单位:叶坚教授课题组
作者:贺靖
审核:叶坚
